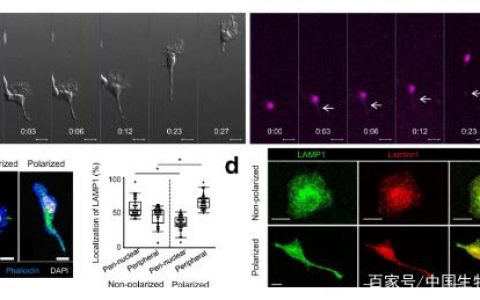
自建立第一个胚胎干细胞(ESC)以来,全能细胞的体外培养在功能上和分子上与具有胚胎和胚外发育潜能的体内卵裂球相当。
2021年5月14日,北京大学杜鹏团队在Cell 在线发表题为“Mouse totipotent stem cells captured and maintained through spliceosomal repression”的研究论文,该研究报告小鼠ESCs剪接体抑制驱动多能到全能状态转换。该研究使用剪接抑制剂Pladienolide B,可以在分子水平上与2细胞和4细胞卵裂球(称为全能卵裂卵球样细胞(TBLC))相比,在全能的ESC上实现稳定的体外培养。
小鼠嵌合检测与单细胞RNA测序(scRNA-seq)结合表明TBLC具有强大的双向发育能力,可产生多种胚胎和胚外细胞谱系。在机制上,剪接体阻遏导致多能基因的广泛剪接抑制,而几乎不含短内含子的全能基因被有效剪接并转录激活。该研究研究提供了一种捕获和维持全能干细胞的方法。
另外,2021年5月5日,北京大学杜鹏及哈佛医学院Richard I. Gregory共同通讯在Nature 在线发表题为“Global miRNA dosage control of embryonic germ layer specification”的研究论文,该研究确定了发育调控的miRNA剂量控制机制,涉及DGCR8的可变转录起始(ATI)。ATI发生在DGCR8 mRNA的茎环下游,绕过小鼠胚胎干(mES)细胞分化过程中的自调节反馈环。删除茎环会导致DGCR8:DROSHA蛋白化学计量失衡,从而导致不可逆的微加工器聚集,减少的primary miRNA加工,降低的成熟miRNA丰度以及脂质代谢mRNA目标的广泛抑制。尽管全局miRNA剂量控制对于mES细胞退出多能性并不是必不可少的,但其失调会通过破坏体外和体内的胚层规格来改变脂质代谢途径并干扰胚胎发育。这种miRNA剂量控制机制在人类中是保守的。该研究结果确定了一个启动子开关,该开关可以平衡微加工器的自动调节和聚集,以精确控制全局miRNA剂量并在早期胚胎发育过程中控制干细胞的命运决定(点击阅读)。

干细胞研究与再生医学,辅助生殖,癌症,代谢紊乱和衰老有着广泛的联系。体外具有高分化潜能的胚胎干细胞(ESCs)是基本且重要的。全能细胞具有最高的发展潜力,通常指哺乳动物的体内受精卵和2细胞和4细胞卵裂球。在早期胚胎发育过程中,全能卵裂球专门化为内部细胞团(ICM)和滋养外胚层(TE),而ICM则产生了胚泡的原始内胚层(PrE)和表皮细胞(EPI)。胚胎植入后,EPI产生包含三个胚层的胚胎组织,而PrE产生内脏内胚层(VE)和顶叶内胚层(PE),最终发展为卵黄囊组织。TE产生胚外组织,例如外胎盘锥(EPC)和胚外外胚层(ExE),并最终形成胎盘。
体外培养的ESC通常来源于ICM,并且能够分化为成年生物的任何细胞类型,称为多能性细胞,其特征在于转录因子的表达,例如POU5F1(OCT4),ZFP42,NANOG和SOX2。最近,据报道,培养的ESC中有很小一部分(0.1%–1%)激活MERVL和MT2转座子以及其他全能基因(例如ZSCAN4s)的表达。两项研究报告了一种新型的扩展型多能干细胞(EPSC),能够实现胚胎和胚外分化,并可以在具有不同化学混合物的培养基中建立和维持。但是,最近的一项研究对EPSC在分子和功能水平上的全能性提出了质疑和怀疑。迄今为止,尚无法获得在分子上和功能上与体内全能卵裂球相似的全能干细胞的体外捕获和维持。
剪接体是具有五个核心亚基和几个辅因子的大分子核糖核蛋白(RNP)复合物,并且是信使RNA(mRNA)剪接和成熟的动态分子机器。最近的研究表明,剪接体还可以直接控制转录的起源,延伸和终止,突出了它们的非剪接独立功能。有趣的是,在许多不同的癌症中,已经确定了几种关键剪接因子的突变在肿瘤发生中起着至关重要的作用。但是,剪接体在干细胞命运转变和早期胚胎发育中可能的生理相关性尚不清楚。
该研究报告小鼠ESCs剪接体抑制驱动多能到全能状态转换。使用剪接抑制剂Pladienolide B,该研究可以在分子水平上与2细胞和4细胞卵裂球(称为全能卵裂卵球样细胞(TBLC))相比,在全能的ESC上实现稳定的体外培养。
编辑:小果果,转载请注明出处:https://www.cells88.com/linchuang/lcyj/3351.html
免责声明:本站所转载文章来源于其他平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请及时告知,我们会在24小时内删除相关信息。
说明:本站所发布的案例均摘录于文献,仅用于科普干细胞与再生医学相关知识,不作为医疗建议。


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫